1. Le batterie agli ioni di litio sono acquose?
La maggior parte delle batterie agli batterie agli ioni di litio non sono batterie acquose. In genere utilizzano elettroliti organici a base di carbonati (come EC/DMC), che hanno un’ampia finestra di stabilità elettrochimica (>4 V), consentendo un’elevata densità energetica. Tuttavia, questi elettroliti sono infiammabili e hanno una scarsa stabilità termica, con conseguenti rischi per la sicurezza.
Le batterie agli ioni di litio acquose (ALIB), invece, utilizzano elettroliti a base di acqua. Questi sistemi sono intrinsecamente più sicuri, ma la loro finestra di tensione operativa è limitata a causa della decomposizione dell’acqua:
- Finestra di stabilità termodinamica: 1.23 V
- Finestra elettrochimica effettiva: ~1.5-2.3 V
A causa di queste limitazioni, le batterie al litio acquose richiedono materiali elettrodici accuratamente abbinati e non possono riutilizzare direttamente i materiali delle batterie agli ioni di litio tradizionali.
2. Un sistema di materiali pratico per le batterie al litio acquose
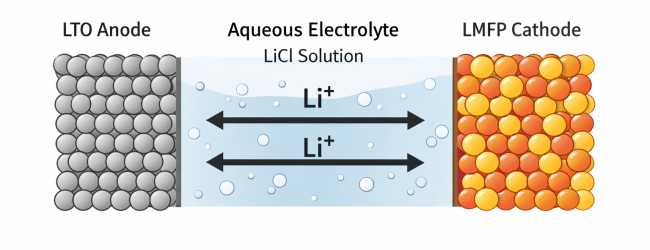
Invece di esplorare complesse combinazioni di materiali, un sistema pratico e ampiamente studiato è costituito da:
- Li₄Ti₅O₁₂ (LTO) – anodo
- LiMnFePO₄ (LMFP) – catodo
- ElettrolitaacquosoLiCl – mezzo conduttivo degli ioni di litio
Questo sistema è comunemente utilizzato nella ricerca accademica, nelle piattaforme di test elettrochimici e nei prototipi di accumulo di energia in fase iniziale grazie al suo equilibrio:
- Stabilità
- Sicurezza
- Disponibilità del materiale
3. Proprietà del materiale del nucleo e parametri elettrochimici
3.1 Proprietà chiave dei materiali nei sistemi di batterie al litio acquose
Per comprendere meglio il ruolo di ciascun materiale, le loro principali proprietà elettrochimiche sono riassunte di seguito.
Titanato di litio (Li₄Ti₅O₁₂, LTO) - Materiale anodico
- Potenziale di funzionamento: ~1,55 V vs Li/Li⁺
- Capacità teorica: 175 mAh/g
- Caratteristica strutturale: Struttura spinelica con caratteristica zero-strain (~0,2% di variazione di volume)
- Ruolo funzionale: Fornisce un inserimento di litio altamente stabile con una lunga durata di ciclo
Fosfato di litio e manganese (LiMnFePO₄, LMFP) - Materiale catodico
- Potenziale di lavoro: ~3,4-3,6 V vs. Li/Li⁺
- Capacità teorica: ~170 mAh/g
- Caratteristiche strutturali: Struttura di fosfato di olivina con forte legame P-O
- Ruolo funzionale: Consente l’immagazzinamento stabile del litio con una dissoluzione ridotta del metallo
Cloruro di litio (LiCl) - Elettrolita acquoso
- Funzione: Mezzo conduttore di ioni di litio
- Solubilità: elevata (~83 g/100 mL a 25°C)
- Caratteristica strutturale: Sale inorganico di litio altamente solubile
- Ruolo funzionale: Garantisce il trasporto del Li⁺ e assicura un funzionamento sicuro e non infiammabile
4. Titanato di litio (Li₄Ti₅O₁₂, LTO): La stabilità strutturale consente batterie acquose di lunga durata

4.1 Caratteristiche elettrochimiche
Iltitanato di litio (Li₄Ti₅O₁₂, LTO) è ampiamente riconosciuto come materiale anodico di riferimento nei sistemi di batterie al litio acquose grazie alla sua eccezionale stabilità strutturale ed elettrochimica. Appartiene alla famiglia degli spinelli e presenta una struttura tridimensionale altamente stabile per la diffusione degli ioni di litio.
L’LTO è spesso descritto come un materiale a “deformazione zero”, ovvero il suo reticolo cristallino non subisce quasi alcuna distorsione strutturale durante l’inserimento e l’estrazione del litio. Questa caratteristica è fondamentale per mantenere la stabilità dei cicli a lungo termine.
I parametri elettrochimici chiave includono:
- Variazione di volume: ~0,2% durante il ciclo
- Altopiano di tensione piatto: ~1,55 V vs Li/Li⁺
- Capacità teorica: 175 mAh/g
- Struttura cristallina: Spinello cubico (gruppo spaziale Fd-3m)
4.2 Perché l'LTO è ideale per i sistemi acquosi
Una delle sfide principali nelle batterie al litio acquose è evitare le reazioni di evoluzione dell’idrogeno (HER) all’anodo. È qui che l’LTO offre un vantaggio decisivo.
Poiché il suo potenziale di lavoro (~1,55 V vs Li/Li⁺) è significativamente più alto di quello della grafite (~0,1 V vs Li/Li⁺), l’LTO opera in sicurezza all’interno della finestra di stabilità elettrochimica dell’acqua.
Questo porta a diversi vantaggi a livello di sistema:
- Soppressione delle reazioni di evoluzione dell’idrogeno negli elettroliti acquosi
- Riduzione delle reazioni collaterali parassite, con conseguente miglioramento dell’efficienza coulombiana
- Maggiore stabilità elettrochimica in caso di cicli ripetuti
- Migliore compatibilità con i sali di litio acquosi (ad esempio, LiCl)
Gli anodi di grafite convenzionali, invece, non sono adatti ai sistemi acquosi a causa del loro basso potenziale operativo, che innesca una rapida decomposizione dell’acqua.
4.3 Prestazioni di ciclo di vita
La robustezza strutturale dell’LTO si traduce direttamente in un’eccellente durata del ciclo, che è uno dei suoi vantaggi più importanti nei sistemi di batterie acquose.
Studi sperimentali hanno dimostrato che:
- Le celle acquose a base di LTO possono raggiungere >1000 cicli stabili di carica-scarica
- In condizioni ottimizzate, la durata dei cicli può estendersi a diverse migliaia di cicli con un minimo decadimento della capacità
- La conservazione della capacità rimane elevata grazie a un degrado strutturale trascurabile
Questo livello di durata rende l’LTO particolarmente adatto alle applicazioni in cui la lunga durata è più importante della massima densità energetica.
4.4 Prospettiva dell'applicazione
Grazie alla sua sicurezza intrinseca e alla stabilità a lungo termine, il titanato di litio (Li₄Ti₅O₁₂, LTO) è ampiamente utilizzato in vari sistemi di batterie acquose e ibride.
Gli scenari applicativi tipici includono:
- Sistemi di accumulo di energia ad alta sicurezza
Soprattutto in ambienti in cui la stabilità termica e l’affidabilità sono fondamentali - Progetti di batterie a ricarica rapida
L’LTO supporta il rapido inserimento degli ioni di litio senza significative sollecitazioni strutturali - Piattaforme di ricerca per batterie agli ioni di litio acquose
Spesso utilizzato come materiale anodico standard nella ricerca e sviluppo accademica e industriale - Sistemi di accumulo su scala di rete e stazionari
Dove la lunga durata del ciclo (>1000-5000 cicli) è prioritaria rispetto alla densità energetica
Dal punto di vista dell’ingegneria dei materiali, l’LTO non è solo una scelta anodica: è un’ancora di stabilità all’interno dei sistemi di batterie al litio acquose, che consente prestazioni costanti in condizioni elettrochimiche difficili.
5. Fosfato di litio e manganese (LiMnFePO₄, LMFP): un catodo bilanciato per stabilità e tensione

5.1 Caratteristiche strutturali ed elettrochimiche
Ilfosfato di ferro e manganese di litio (LiMnFePO₄, LMFP) è un materiale catodico misto di fosfato olivino di metalli di transizione che combina la stabilità strutturale del fosfato di ferro con il contributo di tensione più elevato del manganese.
L’LMFP appartiene alla famiglia dei fosfati olivini, noti per la loro forte struttura polianionica. La presenza di tetraedri PO₄³- forma forti legami covalenti P-O, migliorando significativamente la rigidità strutturale e la stabilità termica.
I principali parametri elettrochimici includono:
- Capacità teorica: ~170 mAh/g
- Tensione operativa: ~3,4-3,6 V vs. Li/Li⁺
- Struttura cristallina: Olivina ortorombica (gruppo spaziale Pnma)
- Meccanismo redox: Coppie Fe²⁺/Fe³⁺ e Mn²⁺/Mn³⁺
Rispetto ai sistemi monocomponente come LiFePO₄, LMFP offre una combinazione equilibrata di tensione e stabilità, che lo rende particolarmente adatto a progetti di batterie compatibili con l’acqua.
5.2 Stabilità in elettroliti acquosi
Una delle sfide principali nei sistemi di batterie al litio acquose è la stabilità chimica dei materiali catodici, soprattutto in caso di cicli ripetuti in elettroliti a base acquosa.
Il fosfato di litio e manganese (LiMnFePO₄, LMFP) presenta chiari vantaggi rispetto ai catodi di ossido stratificato (come NCM o NCA):
- Minore dissoluzione dei metalli di transizione in ambienti acquosi
- Integrità strutturale più forte grazie alla struttura polianionica
- Ridotte reazioni di degradazione superficiale
- Migliore stabilità ai cicli a lungo termine
La stabilità deriva dall’effetto induttivo del gruppo PO₄³-, che stabilizza i legami metallo di transizione-ossigeno e sopprime il rilascio di ossigeno o il collasso strutturale.
Di conseguenza, i materiali a base di fosfato di olivina come LMFP sono ampiamente considerati più adatti per i sistemi elettrolitici acquosi e ibridi rispetto ai catodi stratificati convenzionali.
5.3 Prospettiva dell'applicazione
Grazie alle sue prestazioni elettrochimiche equilibrate e alla sua struttura robusta, il fosfato di litio e manganese (LiMnFePO₄, LMFP) è ampiamente utilizzato sia nella ricerca che nei sistemi di batterie orientati alle applicazioni.
Gli scenari applicativi tipici includono:
- Sistemi di accumulo di energia a lunga durata
In cui la stabilità del ciclo è prioritaria rispetto alla densità di picco dell’energia - Applicazioni di batterie sensibili ai costi
Grazie all’uso di materie prime relativamente abbondanti e meno costose - Sviluppo di materiali catodici sicuri
In particolare nelle batterie acquose agli ioni di litio e nei sistemi ibridi - Piattaforme di batterie acquose di nuova generazione
Dove la compatibilità con gli elettroliti a base acquosa è fondamentale
Dal punto di vista della progettazione del sistema, LMFP funge da affidabile controparte catodica degli anodi LTO, consentendo una configurazione stabile e sicura delle batterie al litio acquose.
6. Elettrolita acquoso di cloruro di litio (LiCl): Trasporto ionico e stabilità del sistema
6.1 Proprietà fisiche e chimiche

Ilcloruro di litio (LiCl) è un sale inorganico di litio altamente solubile, ampiamente utilizzato nei sistemi di batterie acquose come efficace componente elettrolitico.
Grazie alla sua forte natura ionica, il LiCl si dissocia prontamente in acqua per formare ioni Li⁺ e Cl-, consentendo un efficiente trasporto di ioni all’interno dell’elettrolita.
Le caratteristiche principali includono:
- Elevata solubilità: ~83 g / 100 mL a 25°C
- Forte dissociazione ionica: Rapida formazione di portatori di Li⁺
- Elevata conducibilità ionica: Adatto ai sistemi elettrochimici
- Stabilità chimica: Stabile nelle condizioni tipiche delle batterie acquose
Queste proprietà rendono il LiCl una scelta pratica e affidabile per i sistemi di batterie al litio acquose su scala di laboratorio e di ricerca.
6.2 Ruolo elettrochimico
Nelle batterie acquose agli ioni di litio, il cloruro di litio (LiCl) funge da mezzo centrale per il trasporto degli ioni e la stabilità del sistema.
Le sue funzioni principali comprendono:
- Consentire il trasporto continuo di ioni Li⁺ tra il catodo e l’anodo
- Mantenere un ambiente ionico stabile durante i processi di carica e scarica
- Sostenere le reazioni elettrochimiche su entrambi gli elettrodi
- Garantendo un sistema elettrolitico non infiammabile e più sicuro rispetto ai solventi organici
Fornendo una fornitura costante di ioni di litio mobili, LiCl svolge un ruolo fondamentale nel mantenimento delle prestazioni e dell’efficienza complessive della batteria.
6.3 Perché il LiCl viene utilizzato nei sistemi di ricerca
Rispetto a sistemi elettrolitici più complessi, il cloruro di litio (LiCl) è ampiamente utilizzato nella ricerca sulle batterie acquose grazie ai suoi vantaggi pratici:
- Semplicità: Facile da preparare e da maneggiare in soluzioni acquose
- Elevata riproducibilità: Prestazioni coerenti tra gli esperimenti
- Compatibilità con i materiali: Funziona efficacemente con
- Anodi di titanato di litio (Li₄Ti₅O₁₂, LTO)
- Catodi di litio manganese ferro fosfato (LiMnFePO₄, LMFP)
- Costo-efficacia: Facilmente reperibile e adatto a test scalabili
Queste caratteristiche rendono il LiCl un elettrolita ideale per:
- Piattaforme di test elettrochimici
- Prototipazione di batterie al litio acquose
- Valutazione delle prestazioni dei materiali
7. Integrazione a livello di sistema: Come LTO, LMFP e LiCl lavorano insieme
In un sistema completo di batteria al litio acquosa, questi tre materiali funzionano come un’unità elettrochimica coordinata:
- Iltitanato di litio (Li₄Ti₅O₁₂, LTO) agisce come anodo, fornendo un inserimento stabile del litio con un minimo cambiamento strutturale
- Il fosfato di litio e manganese (LiMnFePO₄, LMFP) funge da catodo, consentendo lo stoccaggio reversibile del litio
- Il cloruro di litio (LiCl) funge da elettrolita, facilitando il trasporto di Li⁺ tra gli elettrodi
Meccanismo di funzionamento del sistema
- Durante la carica: Gli ioni Li⁺ migrano da LMFP → LTO
- Durante la scarica: Gli ioni Li⁺ ritornano da LTO → LMFP
Questa interazione coordinata dà luogo a un sistema che è..:
- Strutturalmente stabile
- Elettrochimicamente reversibile
- Più sicuro dei sistemi elettrolitici organici convenzionali
8. Applicazioni pratiche di questo sistema di materiali
Il sistema LTO + LMFP + LiCl non è stato progettato per ottenere la massima densità di energia, ma per:
8.1 Vantaggi principali
- Elevata sicurezza (elettrolita non infiammabile)
- Lunga durata del ciclo (stabilità dell’LTO)
- Basso impatto ambientale
8.2 Scenari di applicazione
- Sistemi di accumulo di energia stazionari
- Integrazione delle energie rinnovabili (tamponamento solare/eolico)
- Test elettrochimici di laboratorio
- Piattaforme di ricerca sui materiali delle batterie
9. Sistema di materiali per batterie completamente acquose ULPMAT
Basandosi sulla struttura dei materiali delle batterie al litio acquose, ULPMAT fornisce una piattaforma di materiali completa e integrata, che consente agli utenti di andare oltre i test su un singolo materiale e di sviluppare un sistema completo.
Invece di acquistare separatamente i singoli componenti, questo approccio favorisce la compatibilità dei materiali, semplifica l’approvvigionamento e velocizza la convalida sperimentale.
9.1 Copertura del materiale
Il sistema di materiali per batterie acquose di ULPMAT comprende una gamma completa di materiali funzionali per tutti i componenti chiave:
- Materiali anodici:
Compreso il titanato di litio (Li₄Ti₅O₁₂, LTO) e altri composti di inserimento a base di titanio progettati per garantire un’elevata stabilità strutturale e una lunga durata dei cicli - Materiali catodici:
Compresi il fosfato di ferro e manganese di litio (LiMnFePO₄, LMFP), il fosfato di ferro e litio (LiFePO₄, LFP) e i relativi materiali a base di fosfato olivino adatti a sistemi compatibili con l’acqua - Materiali elettrolitici:
Compresi il cloruro di litio (LiCl) e altri sali di litio utilizzati per la formulazione di elettroliti acquosi e per i test elettrochimici - Sistemi acquosi estesi:
Materiali di supporto per batterie acquose a base di sodio, come i composti di tipo NASICON e gli analoghi del blu di Prussia
Questa copertura strutturata dei materiali consente agli utenti di progettare, testare e ottimizzare i sistemi di batterie acquose all’interno di un quadro di materiali unificato.
9.2 Vantaggi del sistema
Offrendo un sistema completo di materiali piuttosto che prodotti isolati, ULPMAT consente diversi vantaggi pratici:
- Impostazione sperimentale più rapida
Tutti i materiali chiave sono disponibili all’interno di un sistema coordinato, riducendo la complessità dell’approvvigionamento e i tempi di preparazione - Compatibilità coerente dei materiali
I materiali sono allineati in termini di comportamento elettrochimico, migliorando la stabilità del sistema e la riproducibilità - Transizione scalabile dalla ricerca all’applicazione
Adatto sia per test su scala di laboratorio sia per lo sviluppo di applicazioni in fase iniziale - Maggiore efficienza nello sviluppo
Riduce i tentativi e gli errori nella selezione dei materiali, consentendo di concentrarsi maggiormente sull’ottimizzazione del sistema
10. FAQ: Materiali per batterie acquose al litio
Q1. Le batterie agli ioni di litio acquose sono più sicure di quelle tradizionali?
Sì. Le batterie agli ioni di litio acquose utilizzano elettroliti a base d’acqua, che non sono infiammabili e riducono significativamente il rischio di fuga termica rispetto ai sistemi con elettroliti organici.
Q2. Perché l’LTO è preferito alla grafite nei sistemi di batterie acquose?
L’LTO funziona a un potenziale più elevato (~1,55 V rispetto a Li/Li⁺), che consente di evitare le reazioni di evoluzione dell’idrogeno negli elettroliti acquosi. Al contrario, la grafite opera a potenziali molto più bassi ed è instabile nei sistemi acquosi.
Q3. Cosa rende l’LMFP adatto ai catodi acquosi?
L’LMFP ha una struttura olivina stabile con forti legami P-O, che riduce la dissoluzione dei metalli di transizione in ambienti acquosi e migliora la stabilità dei cicli a lungo termine.
Q4. Il LiCl può essere sostituito da altri sali di litio nelle batterie acquose?
Sì. È possibile utilizzare anche altri sali di litio (come Li₂SO₄ o LiNO₃). Tuttavia, il LiCl è ampiamente scelto per la sua elevata solubilità, la forte conducibilità ionica e la semplicità sperimentale, che lo rendono adatto per la ricerca e la prototipazione.
Q5. Quali sono le principali applicazioni dei sistemi di batterie al litio acquose?
I sistemi di batterie al litio acquose sono utilizzati principalmente in:
- Accumulo di energia stazionario
- Sistemi di tamponamento di energia rinnovabile
- Ricerca sulle batterie su scala di laboratorio
- Prototipazione di batterie sicure
Queste applicazioni beneficiano più della sicurezza e della durata del ciclo che della massima densità energetica.
11. Conclusione
Sebbene la maggior parte delle batterie agli ioni di litio non sia acquosa, i sistemi acquosi al litio rappresentano una chiara direzione verso un accumulo di energia più sicuro e sostenibile.
Tra le numerose combinazioni di materiali, il sistema basato su:
- LTO (Li₄Ti₅O₁₂)
- LMFP (LiMnFePO₄)
- Elettrolita LiCl
offre una soluzione pratica, supportata dalla ricerca e scalabile.
Con la crescente domanda di sicurezza e sostenibilità, questo sistema di materiali sta diventando una piattaforma importante per lo sviluppo e la ricerca sulle batterie di prossima generazione.